Phương pháp giải bài xích tập
Phương pháp giải bài xích tập ancol
Các dạng bài bác tập ancol bao gồm lời giải6 dạng bài tập về Ancol trong đề thi Đại học bao gồm giải chi tiết
Phương pháp giải bài tập làm phản ứng đốt cháy ancol
Các dạng bài bác tập ancol và phương thức giải bài bác tập
Như những em đã biết, ancol là những hợp chất hữu tuy nhiên trong phân tử gồm chứa team -OH links với nguyên tử C no (C sp3) của gốc hiđrocacbon. Những lý thuyết về ancol họ đã được khám phá trước đó, bây chừ chúng ta sẽ khám phá xem liệu là vào phân tử bao gồm chứa team -OH như vậy, thì vẫn cócác dạng bài tập ancol này nhé!Nội dung chính
Các dạng bài bác tập ancolPhương pháp giải bài xích tập
Dạng 1: Viết đồng phân hotline tên ancol
Dạng 2: xác minh CTPT của ancol
Dạng 3: Ancol bóc nước sản xuất Anken
Dạng 4: Ancol tách nước trong điều kiện thích hợp
Dạng 5: Ancol tách nước tạo Este
Dạng 6: phản ứng thoái hóa không hoàn toàn của ancol
Dạng 7: bội nghịch ứng oxi hóa hoàn toàn (phản ứng cháy)
Các dạng bài bác tập ancol
Dạng 1: Viết đồng phân gọi tên ancol
Dạng 2: khẳng định CTPT của ancol
Dạng 3: Ancol tách bóc nước tạo Anken
Dạng 4: Ancol bóc tách nước trong điều kiện thích hợp
Dạng 5:Ancol bóc tách nước tạo nên Este
Dạng 6: phản bội ứng oxi hóa không hoàn toàn của ancol
Dạng 7: bội phản ứng oxi hóa trọn vẹn (phản ứng cháy)
Phương pháp giải bài xích tập
Dạng 1: Viết đồng phân hotline tên ancol
– tất cả 2 biện pháp gọi tên ancol
+Tên nơi bắt đầu – chức:“Ancol” + tên cội hidrocacbon + “ic”
Ví dụ: CH3CH2OH là ancol etylic
+ Tên rứa thế:Tên hidrocacbon + số chỉ vị trí nhóm OH + “ol”
Ví dụ: CH3CH2OH là etanol
– các ancol mang tên gọi thông thường phổ cập nhất là:
CH2OH-CH2OH: Etilen glicol
CH2OH-CHOH-CH2OH: Glixerol hoặc glixerin
Chú ý:
(CH3)2CH2– là gốc isopropyl
CH2=CH-CH2– là gốc anlyl
C6H5CH2– là nơi bắt đầu bezyl
Ví dụ:Gọi tên các ancol sau theo tên thông thường: C6H5CH2OH, CH2=CH-CH2OH, CH3CH2CH2OH
Trả lời:
C6H5CH2OH:Ancol benzylic
CH2=CH-CH2OH: Ancol anlylic
CH3CH2CH2OH: Ancol propylic
Dạng 2: xác minh CTPT của ancol
– tự công thức đơn giản hoặc cách làm thực nghiệm, ta suy luận phụ thuộc công thức bao quát của ancol (no đối chọi chức, không no đối kháng chức, đa chức…)
– vào CTTQ: Cx
Hy
Oz
Ta có: y = 2x+2 cùng y luôn luôn chẵn.
Bạn đang xem: Các dạng bài tập về ancol và cách giải
– trong ancol đa chức thì số nhóm OH > 1
Ví dụ 1:Cho Na phản nghịch ứng hoàn toàn với 18,8 gam hỗn hợp hai ancol kế tiếp nhau trong hàng đồng đẳng của ancol etylic, thu được 5,6 lít khí H2( sinh hoạt đktc). Xác định CTPT của nhị ancol?
Lời giải:
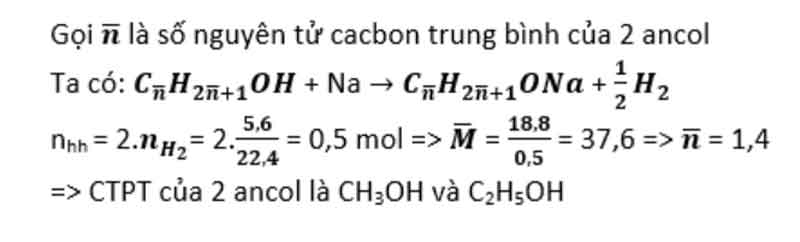
Ví dụ 2:Cho 15,6 gam hỗn hợp hai ancol đối kháng chức, kế tiếp nhau trong dãy đồng đẳng công dụng hết với 9,2 gam Na, chiếm được 24,5 gam hóa học rắn. Khẳng định CTPT của nhì ancol?
Lời giải:

Dạng 3: Ancol tách bóc nước sản xuất Anken
+ Ancol bóc nước chế tạo ra 1 anken tốt nhất thì ancol sẽ là ancol no đối kháng chức, bậc 1
+ Áp dụng định công cụ bảo toàn khối lượng có: mancol= manken+ mnước
+nancol= nanken= nnước
+ hỗn hợp X tất cả 2 ancol bóc tách nước thu được hỗn hợp Y gồm các olefin thì lượng CO2thu được lúc đốt cháy X bằng khi đốt cháy Y
Ví dụ 1:Tách nước hoàn toàn từ tất cả hổn hợp X bao gồm 2 ancol A, B ta được tất cả hổn hợp Y gồm những olefin. Ví như đốt cháy hoàn toàn hỗn đúng theo X thì thu được 1,76 g CO2. Khi đốt cháy trọn vẹn Y thì tổng khối lượng nước với CO2tạo ra là?
Lời giải
Áp dụng định mức sử dụng bảo toàn yếu tắc cacbon ta có
Lượng CO2thu được khi đốt cháy Y bằng khi đốt cháy X = = 0,04 mol
Mà Y là lếu láo hợp các olefin đề xuất số mol H2O = số mol CO2= 0,04 mol
Vậy tổng khối lượng CO2và H2O thu được là : 0,04 . 18 + 1,76 = 2,48 g
Ví dụ 2:Khi triển khai phản ứng bóc tách nước đối với ancol X, chỉ thu được 1 anken duy nhất. Oxi hoá trọn vẹn một lượng chất X nhận được 5,6 lít CO2(đktc) và 5,4 gam H2O. Tất cả bao nhiêu cách làm cấu tạo cân xứng với X?
Lời giải
X bị tách nước chế tác 1 anken X là ancol no, 1-1 chức với chỉ có 1 hướng tách
Công thức phân tử của X là Cn
H2n+1OH ;
Có nancol= n
HO– n
CO= 0,05 mol
Và n = 5 . đề xuất công thức phân tử của X là C5H11OH
Công thức cấu trúc của X là
CH3– CH2– CH2– CH2– CH2OH
CH3– CH(CH3) – CH2– CH2OH
CH3– CH2– CH(CH3) – CH2OH
Dạng 4: Ancol bóc nước trong đk thích hợp
Phương pháp giải nhanh
Ancol X bóc tách nước trong điều kiện thích hợp tạo thành phầm hữu cơ Y thì
+ giả dụ tỉ khối của Y so với X bé dại hơn 1 thì Y là anken cùng d
Y/X = 14 / (14n +18)
+ trường hợp tỉ khối của Y so với X to hơn 1 thì Y là ete với d
Y/ X= (2R+16) / (R+17)
Ví dụ:Đun rét một ancol solo chức X với hỗn hợp H2SO4 sệt trong điều kiệnthích vừa lòng sinh ra chất hữu cơ Y, tỉ khối của X đối với Y là 1,6428. Công thức phântử của Y là
Lời giải
Vìd
X/Y= 1,6428 nênd
Y/X= 1/1,6428
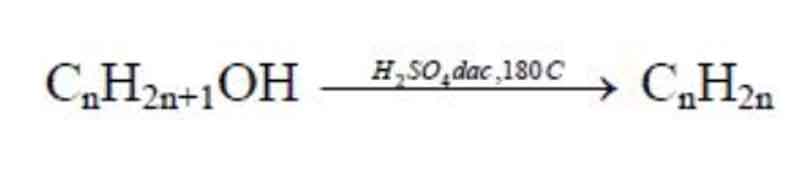
d
Y/X = 14n / (14n+18) = 1/1,6428 => n=2
Vậy công thức phân tử của X là C2H6O
Dạng 5: Ancol bóc nước sản xuất Este
+ tất cả hổn hợp 2 ancol tách nước tạo ra 3 ete, 3 ancol bóc nước tạo ra 6 ete
+ áp dụng định chính sách bảo toàn trọng lượng có: mancol= manken+ mnước
+ nete= nnước= nancol
+ các ete có số mol đều nhau thì những ancol cũng có số mol bởi nhau
+ tổng cộng nguyên tử cacbon trong ancol bằng số nguyên tử vào ete
Ví dụ 1:Đun nóng lếu hợp bao gồm 2 ancol đối kháng chức, mạch hở, kế tiếp nhau trong hàng đồng đẳng với H2SO4đặc nghỉ ngơi 140o
C. Sau khi các bội nghịch ứng kết thúc, thu được 6 gam hỗn hợp 3 ete với 1,8 gam nước. Phương pháp phân tử của 2 ancol bên trên là?
Lời giải
Ta bao gồm nancol= 2nnước= 2. = 0,2 mol
áp dụng định phép tắc bảo toàn khối lượng có : mancol= mete+ mnước= 6 + 1,8 = 7,8 gam
Gọi công thức chung của 2 ancol OH. Suy ra = = 39= 39 – 17 = 22
Mà 2 ancol là đồng đẳng tiếp tục nên 2 ancol đề nghị là CH3OH và C2H5OH
Ví dụ 2:Cho V lít (đktc) tất cả hổn hợp khí bao gồm 2 olefin liên tiếp nhau trong hàng đồng đẳng thích hợp nước (xúc tác H2SO4đặc), thu được 12,9 gam tất cả hổn hợp A tất cả 3 ancol. Đun nóng các thành phần hỗn hợp A vào H2SO4đặc ở 140o
C chiếm được 10,65 gam hỗn hợp B tất cả 6 ete khan. Phương pháp phân tử của 2 anken là?
Lời giải
Áp dụng định luật bảo toàn cân nặng ta có
mnước= mancol– mete= 12,9 – 10,65 = 2,25 gam; nnước= = 0,125 mol
Ta tất cả nancol= 2nnước= 2. 0,125= 0,25 mol. Gọi bí quyết chung của 2 ancol là OH
Suy ra = = 51,6= 51,6 – 17 = 34,6. Nhưng 2 anken là đồng đẳng tiếp tục nên 3 ancol tất cả 2 ancol là đồng phân của nhau với cũng là những ancol đồng đẳng liên tiếp. Phải 3 ancol là C2H5OH và C3H7OH 2 anken là C2H4và C3H6.
Dạng 6: phản ứng thoái hóa không trọn vẹn của ancol
Khi đun cho nóng với Cu
O thì:
– Ancol bậc I bị oxi hóa thành anđehit.
– Ancol bậc II bị oxi trở thành xeton.
– Ancol bậc III không trở nên oxi hóa.
Với ancol no, 1-1 chức mạch hở ta có thể viết dưới dạng:
Cn
H2n+2O + Cu
O→Cn
H2n
O + Cu + H2O
Ví dụ1:Cho m gam ancol no, đối kháng chức mạch hở X đi qua bình đựng Cu
O dư, nóng. Sau khi phản ứng xảy ra hoàn toàn, thấy gồm 1,6 gam Cu
O đang phản ứng. Tất cả hổn hợp hơi Y sau bội nghịch ứng có tỷ khối đối với H2 là 15,5. Xác định CTPT của X?
Lời giải

Ví dụ 2:Cho m gam một ancol no, đơn chức X qua bình Cu
O dư đun nóng. Sau khoản thời gian phản ứng trả toàn, trọng lượng chất rắn vào bình bớt 0,32 gam. Tất cả hổn hợp hơi thu được có tỉ khối cùng với hiđro là 15,5. Giá trị của m là
Lời giải
Áp dụng định phương tiện bảo toàn trọng lượng và nhân tố ta có
nancol= nanđehit = = = 0,02 mol
Ta bao gồm sơ đồ: R – CH2OH + Cu
O→R – mang lại + Cu + H2O
0,02 mol 0,02 mol 0,02 mol
Ta có: M = 15,5 x 2 = 31
Suy ra R = 15 yêu cầu ancol X là CH3OH
Vậy trọng lượng ancol X là : m = 0,02 . 32 = 0,64 gam.
Dạng 7: bội nghịch ứng oxi hóa trọn vẹn (phản ứng cháy)
Phản ứng đốt cháy ancol:
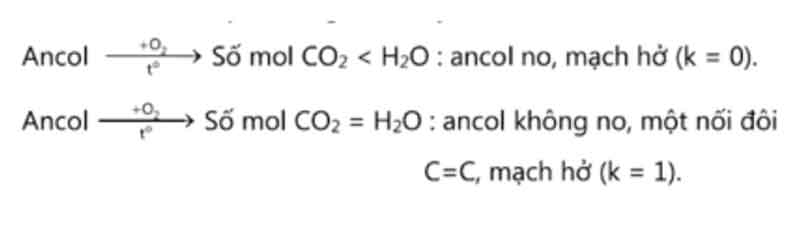
Ví dụ 1:Đốt cháy hoàn toàn ancol X thu được các thành phần hỗn hợp V lít(đktc) CO2và 1,08 gam H2O. Dẫn toàn cục lượng CO2này vào 2 lít hỗn hợp Na
OH 0,1M thu được hỗn hợp Na
OH bao gồm nồng độ là 0,05M. Khẳng định công thức hàng đồng đẳng X, biết X là ancol đối chọi chức.
Lời giải

Phương pháp giải bài tập ancol
Dạng 1: Viết đồng phân điện thoại tư vấn tên ancol
Có 2 phương pháp gọi tên ancolTên cội – chức: “Ancol” + tên cội hidrocacbon + “ic”Ví dụ: CH3CH2OH là ancol etylic
Tên núm thế: tên hidrocacbon + số chỉ vị trí nhóm OH + “ol”Ví dụ: CH3CH2OH là etanol
Dạng 2: xác định CTPT của ancol
Từ công thức đơn giản dễ dàng hoặc cách làm thực nghiệm, ta suy luận nhờ vào công thức tổng quát của ancol (no đơn chức, không no solo chức, nhiều chức…)Trong CTTQ: CxHyOzTa có: y = 2x+2 cùng y luôn luôn chẵn.Trong ancol đa chức thì số nhóm OH > 1Dạng 3: Ancol tách bóc nước tạo ra Anken
Ancol bóc tách nước và tạo thành 1 anken tuyệt nhất thì ancol chính là ancol no 1-1 chức, bậc 1.Áp dụng định phương tiện bảo toàn trọng lượng có:mancol=manken+mH2Onancol=nanken=nH2OHỗn hòa hợp X tất cả 2 ancol tách bóc nước thu được các thành phần hỗn hợp Y gồm những olefin thì lượng CO2 thu được lúc đốt cháy X bằng khi đốt cháy Y.Dạng 4: Ancol tách nước trong đk thích hợp
Phương pháp giải nhanh:
Ancol X tách bóc nước vào điều kiện tương thích để tạo sản phẩm hữu cơ Y thì:

Dạng 5: Ancol bóc nước tạo nên Este
Hỗn hợp 2 ancol bóc tách nước sinh sản 3 ete, 3 ancol bóc tách nước chế tác 6 ete
Áp dụng định phép tắc bảo toàn khối lượng có:mancol=manken+mH2Onete=nH2O=nancol***Lưu ý:
Các ete tất cả số mol đều bằng nhau thì các ancol cũng có số mol bởi nhauTổng số nguyên tử cacbon vào ancol thông qua số nguyên tử vào ete
Dạng 6: phản ứng thoái hóa không trọn vẹn của ancol
Khi làm cho nóng với Cu
O thì:
Với ancol no, 1-1 chức mạch hở thì ta rất có thể viết dưới dạng:
Cn
H2n+2O+Cu
O→Cn
H2nO+Cu+H2O
Dạng 7: làm phản ứng oxi hóa hoàn toàn (phản ứng cháy)
Phản ứng đốt cháy ancol:
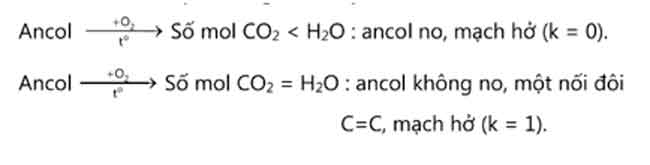
Các dạng bài xích tập ancol tất cả lời giải
Bài tập ancol phenol
Bài 1: Đốt cháy trọn vẹn 1,52 gam một ancol nhận được 1,334 lít khí cacbonic (đktc) với 1,44 gam nước. Bí quyết phân tử của X là gì?
Cách giải
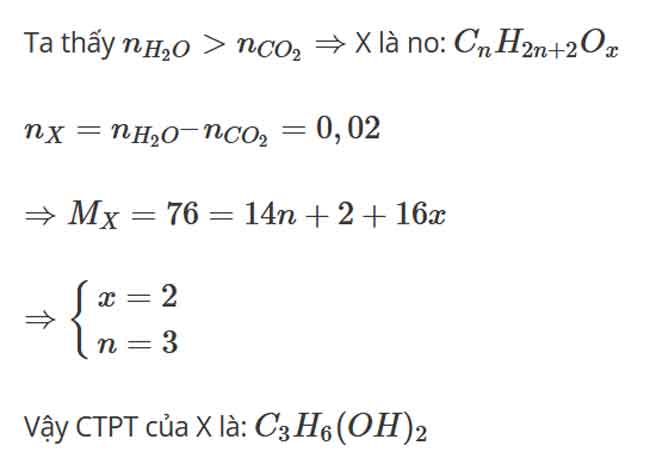
Bài 2: Hỗn hợp X tất cả 3 rượu no 1-1 chức AOH, BOH, ROH. Đun nóng X với hỗn hợp axit sunfuric sệt ở ánh sáng 1800 độ C thu được nhì olefin. Còn mặt khác đun lạnh 132,8 gam tất cả hổn hợp X cùng với axit sunfuric quánh ở 1400 độ C thu được 111,2 gam tất cả hổn hợp este tất cả số mol bởi nhau.
Tìm CTCT của những ancol. Biết rằng các rượu này đều có từ 2 cacbon trở lên.
Cách giải
Vì những rượu này đều sở hữu từ 2 cacbon trở lên nhưng mà khử nước chỉ tạo nên 2 olefin. Suy ra có 2 rượu là đồng phân của nhau.
Giả sử AOH với BOH là đồng phân.

Bài tập dẫn xuất halogen ancol phenol
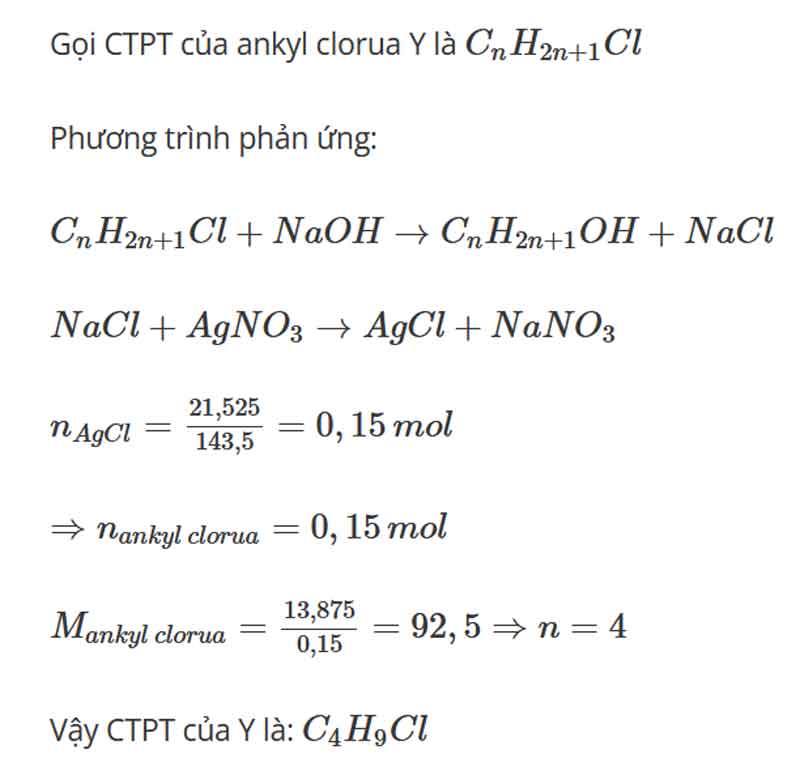
Bài 3: sắp tới xếp năng lực phản ứng núm nguyên tử halogen của các chất sau đây theo trang bị tự sút dần: CH3CH2CH2Cl,CH3CH2CH2Br,CH3CH2CH2F,CH3CH2CH2I
Cách giải
CH3CH2CH2I
Một số bài bác tập trắc nghiệm ancol phenol
Câu 1: Dãy chất được xếp theo sản phẩm tự tăng dần đều nhiệt độ sôi là:
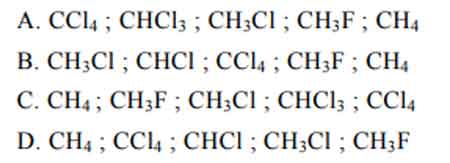
Câu 2: Để nhận biết các chất CH3−CH2−Cl,CH3−CH2−Br,CH3−CH2−I tín đồ ta dùng:
Bột Mg (xúc tác este khan)Dung dịch AgNO3Dung dịch NaOHDung dịch HBr
Câu 3: Để phân biệt tía lọ đựng cha chất là butyl clorua, anlyl clorua, m-điclobenzen bạn ta dùng:
Dung dịch AgNO3Dung dịch NaOH và dung dịch brom
Dung dịch Na
OH và dung dịch AgNO3Dung dịch brom
Câu 4: Teflon là một trong polome bền với nhiệt độ tới bên trên 300 độ C nên được dùng làm bịt phủ chống bám dính cho xoong, chảo, thùng chứa. Teflon được tổng hòa hợp từ:
CH2=CHClCHF=CHFCH2=CHFCF2=CF2Câu 5: cách thức điều chế nào dưới đây giúp ta thu được 2-clobutan tinh khiết hơn cả?
Butan tác dụng với clo, chiếu sáng, tỉ lệ thành phần 1:1But-2-en tính năng với hiđro cloruaBut-1-en chức năng với hiđro clorua
Chỉ gồm một chất có tác dụng làm mất màu hỗn hợp brom
Đáp án
Câu 1 – C
Câu 2 – C
Câu 3 – B
Câu 4 – D
Câu 5 – B
6 dạng bài bác tập về Ancol trong đề thi Đại học có giải đưa ra tiết
Dạng 1: Ancol bóc tách nước
Phương pháp:
Ancol bóc nước 170o, H2SO4→ anken + H2O
nancol = n
H2O = nanken
Ancol bóc tách nước 140o, H2SO4→ ete + H2O
nete = n
H2O = 1/2 nancol
số ete chiếm được từ nancol = (n.(n+1))/2
Sử dụng định quy định bảo toàn khối lượng: mancol = manken(ete) + m
H2O
Ví dụ minh họa
Ví dụ 1 : Đun 132,8 gam các thành phần hỗn hợp 3 rượu no, đối chọi chức với H2SO4 sệt ở 140o
C thu được lếu láo hợp các ete có số mol bằng nhau và có khối lượng là 111,2 gam. Số mol của mỗi ete trong các thành phần hỗn hợp là bao nhiêu ?
A. 0,1 mol. B. 0,15 mol. C. 0,4 mol. D. 0,2 mol.
Hướng dẫn giải:
Ta hiểu được cứ 3 một số loại rượu tách nước ở đk H2SO4 đặc, 140o
C thì sinh sản thành 6 loại ete và bóc tách ra 6 phân tử H2O.
Theo ĐLBTKL ta có
m
H2O = mrượu – mete = 132,8 – 111,2 = 21,6g
⇒ n
H2O = 1,2 mol = nete
nmỗi ete = 1,2/6 = 0,2 mol ⇒ Đáp án D
Ví dụ 2 : bóc tách nước láo lếu hợp có ancol etylic cùng ancol Y chỉ tạo nên 2 anken. Đốt cháy thuộc số mol từng ancol thì lượng nước sinh ra từ ancol này bằng 5/3 lần lượng nước ra đời từ ancol kia. Công thức cấu trúc của Y là:
A. CH3-CH2-CH2-OH. B. CH3-CH(OH)-CH3.
C. CH3-CH2-CH2-CH2-OH. D. CH3-CH2-CH(OH)-CH3.
Hướng dẫn giải:
Gọi công thức ancol Y là: Cn
H2n+2O ( đáp án toàn bộ là ancol no đối kháng chức)
C2H6O → 3H2O
Cn
H2n+2O → (n+1)H2O
Ta có: (n+1)/3 = 5/3 ⇒ n = 4: C4H10O
Tách nước hỗn hợp bao gồm ancol etylic cùng ancol Y chỉ tạo thành 2 anken
⇒ Công thức kết cấu của Y: CH3-CH2-CH2-CH2-OH
⇒ Đáp án C
Ví dụ 3 : thực hiện phản ứng tách nước một rượu solo chức X ở đk thích hợp. Sau khoản thời gian phản ứng xảy ra trọn vẹn thu được chất hữu cơ Y tất cả tỉ khối so với X là 37/23. Công thức phân tử của X là :
A. CH3OH. B. C3H7OH. C. C4H9OH. D. C2H5OH.
Hướng dẫn giải:
Vì MY/MX > 1 nên đấy là phản ứng bóc tách nước tạo thành ete.
Đặt công thức phân tử của ancol X là ROH.
Phương trình phản nghịch ứng :
2ROH → ROR + H2O
(X) (Y)
Theo đưa thiết ta bao gồm :
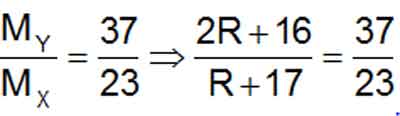
=> R = 29 => R: C2H5
Vậy ancol X là C2H5OH ⇒ Đáp án D
Dạng 2: Ancol tính năng với Na
Phương pháp:
2R(OH)n + 2n
Na → 2R(ONa)n + n
H2
+ sử dụng định chính sách bảo toàn khối lượng, tăng sút khối lượng, bảo toàn nguyên tố
Ví dụ minh họa
Ví dụ 1 : đến 0,1 lít rượu cồn etylic 95o công dụng với mãng cầu dư thu được V lít khí H2 (đktc). Hiểu được ancol etylic nguyên chất có trọng lượng riêng là 0,8 g/ml, cân nặng riêng của nước là 1 g/ml. Quý giá của V là :
A. 43,23 lít. B. 37 lít. C. 18,5 lít. D. 21,615 lít.
Hướng dẫn giải:
Trong 0,1 lít hễ etylic 95o có:
Số ml C2H5OH nguyên chất = 0,1.1000.0,95= 95 ml; khối lượng C2H5OH nguyên hóa học = 95.0,8 = 76 gam; số mol C2H5OH = 76/46 mol.
Số ml nước = 5 ml; trọng lượng nước = 5.1 = 5 gam; số mol nước = 5/18 mol.
Phương trình bội nghịch ứng của na với hỗn hợp ancol :
2H2O + 2Na → 2Na
OH + H2 (1)
2C2H5OH + 2Na → 2C2H5ONa + H2 (2)
Theo phương trình (1), (2) và giả thiết ta tất cả :
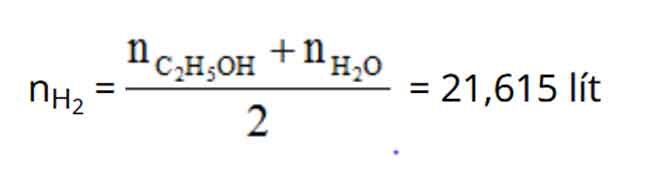
⇒ Đáp án D.
Ví dụ 2 : 13,8 gam ancol A tính năng với mãng cầu dư giải hòa 5,04 lít H2 làm việc đktc, biết MA 3OH. B. C2H5OH. C. C3H6(OH)2. D. C3H5(OH)3.
Hướng dẫn giải:
Đặt phương pháp của ancol là R(OH)n.
Phương trình bội nghịch ứng :
2R(OH)n + 2Na → 2R(ONa)n + n
H2 (1)
13,8/(R+17n) → 13,8/(R+17n). N/2 (mol)
Theo (1) với giả thiết ta bao gồm : n
H2 = 13,8/(R+17n). N/2 = 0,225 mol
⇒ R = 41/3n ⇒ n = 3; R = 41
Vậy A có công thức kết cấu thu gọn gàng là C3H5(OH)3
⇒ Đáp án D
Dạng 3: Ancol bị oxi hóa không hoàn toàn
Phương pháp:
+ Ancol bậc 1 lúc bị oxi hóa vì chưng Cu
O (to) mang lại ra sản phẩm là anđehit.
RCH2OH + Cu
O to→ RCHO + Cu↓ + H2O
+ Ancol bậc hai khi bị oxi hóa vày Cu
O (to) mang lại ra thành phầm là xeton.
R–CH(OH)–R’ + Cu
O to→ R–CO–R’ + Cu↓ + H2O
+ Ancol bậc III cạnh tranh bị oxi hóa.
mc/r giảm = m
Cu
O (phản ứng) – m
Cu (tạo thành)
Ví dụ minh họa
Ví dụ 1 : thoái hóa 6 gam ancol đối chọi chức A bằng oxi không khí (có xúc tác với đun nóng) thu được 8,4 gam tất cả hổn hợp anđehit, ancol dư và nước. Tỷ lệ A bị oxi hóa là :
A. 60%. B. 75%. C. 80%. D. 53,33%.
Hướng dẫn giải:
Đặt công thức của ancol là RCH2OH.
Xem thêm: Cuốn Tiểu Thuyết Đồi Gió Hú, 'Đồi Gió Hú': Mối Tình Dữ Dội Và Đau Đớn
Số mol O2 vẫn tham gia bội nghịch ứng là : n
O2 = (8,4-6)/32 = 0,075 mol
Phương trình phản ứng :
2RCH2OH + O2 → 2RCHO + 2H2O (1)
0,15 0,075 (mol)
Theo (1) ta thấy số mol RCH2OH đang phản ứng là 0,15 mol, theo giả thiết sau bội nghịch ứng ancol còn dư phải ta suy ra số mol ancol thuở đầu phải to hơn 0,15 mol.
⇒ 6/MA > 0,15 ⇒ MA 3OH.
H% = 0,15.32/6.100% = 80%
⇒ Đáp án C
Ví dụ 2 : mang lại m gam một ancol (rượu) no, 1-1 chức X qua bình đựng Cu
O (dư), nung nóng. Sau khi phản ứng hoàn toàn, cân nặng chất rắn vào bình sút 0,32 gam. Tất cả hổn hợp hơi thu được tất cả tỉ khối đối với hiđro là 15,5. Cực hiếm của m là :
A. 0,92. B. 0,32. C. 0,64. D. 0,46.
Hướng dẫn giải:
Đặt công thức phân tử của ancol no, 1-1 chức X là : Cn
H2n + 2O
Phương trình làm phản ứng :
Cn
H2n + 2O + Cu
O → Cn
H2n
O + H2O + Cu (1)
x x → x → x → x (mol)
mc/r sút = m
Cu
O – m
Cu = 80x – 64x = 0,32 => x = 0,02
Hỗn đúng theo hơi gồm Cn
H2n
O với H2O tất cả M=15,5.2 = 31 và n = 0,02.2 = 0,04 mol.
Áp dụng định phép tắc bảo toàn trọng lượng ta bao gồm :
mancol = mhỗn thích hợp hơi + m
Cu – m
Cu
O
mancol = 0,04.31 + 0,02,64 – 0,02.80 = 0,92 gam
⇒ Đáp án A
Dạng 4: Đốt cháy ancol
Phương pháp:
Cn
H2n+1OH + 3n/2O2 to→ n
CO2 + (n+1)H2O
Cn
H2n+2-b(OH)b + (3n+1-b)/2O2 to→ n
CO2 + (n+1)H2O
Chú ý: Ancol no ⇒ n
CO2 > n
H2O;
nancol = n
H2O – n
CO2
Ví dụ minh họa
Ví dụ 1 : Đốt cháy trọn vẹn 0,2 mol một ancol X no, mạch hở cần vừa đủ 17,92 lít khí O2 (ở đktc). Mặt khác, nếu mang lại 0,1 mol X công dụng vừa đầy đủ với m gam Cu(OH)2 thì chế tạo thành hỗn hợp có màu xanh lá cây lam. Quý giá của m và tên gọi của X tương ứng là :
A. 9,8 cùng propan-1,2-điol. B. 4,9 cùng propan-1,2-điol.
C. 4,9 cùng propan-1,3-điol. D. 4,9 với glixerol
Hướng dẫn giải:
Đặt bí quyết phân tử của ancol no X là Cn
H2n + 2Ox (x n).
Phương trình bội phản ứng :
Cn
H2n+2Ox + (3n+1-x)/2O2 to→ n
CO2 + (n+1)H2O (1)
0,2 → (3n+1-x)/2 .0,2 (mol)
⇒ (3n+1-x)/2 .0,2 = 0,8 mol ⇒ 3n – x = 7
⇒ x = 2; n = 3
Vậy bí quyết phân tử của ancol X là C3H8O2 xuất xắc C3H6(OH)2. Bởi X công dụng được với Cu(OH)2 tạo ra dung dịch màu xanh lá cây lam buộc phải X phải có 2 team OH gần cạnh nhau, ancol X có tên là propan-1,2-điol.
Phương trình phản nghịch ứng của propan-1,2-điol cùng với Cu(OH)2 :
2C3H6(OH)2 + Cu(OH)2 →
0,1 0,05 (mol)
Theo (2) và giả thiết ta thấy khối lượng Cu(OH)2 bội phản ứng là :
m
Cu(OH)2 = 0,05.98 = 4,9g
⇒ Đáp án B.
Ví dụ 2 : Đốt cháy hoàn toàn a gam hỗn hợp hai rượu no, đối chọi chức liên tiếp trong hàng đồng đẳng chiếm được 3,584 lít CO2 ngơi nghỉ đktc với 3,96 gam H2O. Tính a và xác minh CTPT của những rượu.
A. 3,32 gam ; CH3OH và C2H5OH. B. 4,32 gam ; C2H5OH với C3H7OH.
C. 2,32 gam ; C3H7OH và C4H9OH. D. 3,32 gam ; C2H5OH với C3H7OH.
Hướng dẫn giải:

⇒ Đáp án D.
Ví dụ 3 : Đốt cháy hoàn toàn m gam tất cả hổn hợp X gồm tía ancol (đơn chức, thuộc thuộc dãy đồng đẳng), thu được 8,96 lít khí CO2 (đktc) cùng 11,7 gam H2O. Phương diện khác, nếu nấu nóng m gam X với H2SO4 sệt thì tổng trọng lượng ete về tối đa chiếm được là:
A. 5,60 gam. B. 6,50 gam. C. 7,85 gam. D. 7,40 gam.
Hướng dẫn giải:
n
CO2 = 0,4 mol; n
H2O = 0,65 mol
n
H2O > n
CO2 ⇒ ancol no; nancol = n
H2O – n
CO2 = 0,25 mol
Gọi công thức chung của 3 ancol là:
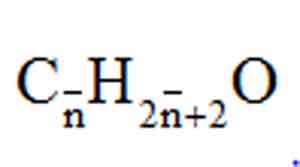
n
O (ancol) = nancol = 0,25 mol
m
X = m
C + m
H + m
O = 0,4.12 + 0,65.2 + 0,25.16 = 10,1g
Khi tách nước: n
H2O = 50% nete = 0,125 mol
Bảo toàn khối lượng: mete = mancol – m
H2O = 10,1 – 0,125.18 = 7,85g
⇒ Đáp án C
Dạng 5: Ancol bội nghịch ứng cùng với axit
Phương pháp:
+ Trong bội nghịch ứng của ancol cùng với axit vô sinh (HCl, HBr) thì bản chất phản ứng là team OH của phân tử ancol bội phản ứng với nguyên tử H của phân tử axit.
R – OH + H– Brđặc to→ RBr + H2O
+ Trong phản nghịch ứng của ancol với axit hữu cơ (phản ứng este hóa) thì thực chất phản ứng là nhóm OH của phân tử axit phản nghịch ứng cùng với nguyên tử H trong nhóm OH của phân tử ancol.
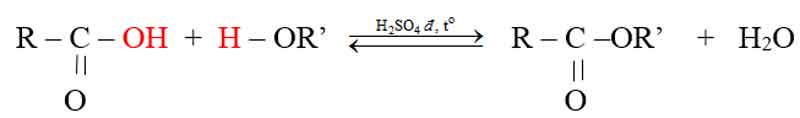
Chú ý:
+ bội nghịch ứng este hóa là phản bội ứng thuận nghịch ⇒ H% Ví dụ minh họa
Ví dụ 1 : Đun nóng ancol A với hỗn hợp Na
Br cùng H2SO4 đặc thu được chất hữu cơ B, 12,3 gam hơi chất B chỉ chiếm một thể tích bởi thể tích của 2,8 gam N2 sinh sống cùng ánh nắng mặt trời 560o
C, áp suất 1 atm. Oxi hoá A bởi Cu
O nung nóng thu được hợp chất hữu cơ có tác dụng làm mất màu dung dịch nước brom. CTCT của A là :
A. CH3OH. B. C2H5OH.
C. CH3CHOHCH3. D. CH3CH2CH2OH
Hướng dẫn giải:
Phương trình phản bội ứng :
Na
Br + H2SO4 → Na
HSO4 + HBr (1)
ROH + HBr → RBr + H2O (2)
(A)(B)
Theo những phản ứng và giả thiết ta bao gồm :
n
RBr = n
N2 = 2,8/28 = 0,1 mol
=> MRBr = 12,3/0,1 = 123 gam/mol => R = 43
⇒ R là C3H7–
Vậy ancol A là C3H7OH. Vì oxi hóa A bởi Cu
O chiếm được hợp chất hữu cơ có chức năng làm mất màu nước Br2 cần công thức cấu trúc của A là CH3CH2CH2OH.
CH3CH2CH2OH + Cu
O → CH3CH2CHO (3)
CH3CH2CHO + Br2 + H2O → CH3CH2COOH + 2HBr (4)
⇒ Đáp án D
Ví dụ 2 : Trộn trăng tròn ml đụng etylic 92o với 300 ml axit axetic 1M thu được hỗn hợp X. Mang lại H2SO4 quánh vào X rồi nấu nóng, sau một thời gian thu được 21,12 gam este. Biết khối lượng riêng của ancol etylic nguyên chất là 0,8 gam/ml. Công suất phản ứng este hoá là :
A. 75%. B. 80%. C. 85%. D. Hiệu quả khác.
Hướng dẫn giải:
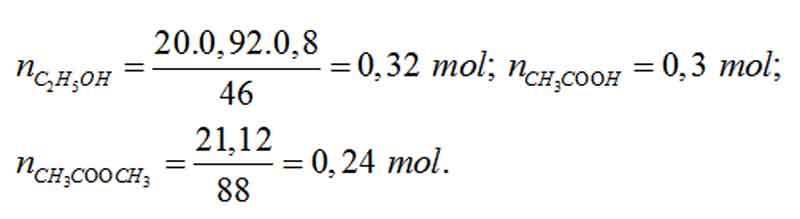
Phương trình làm phản ứng :
CH3COOH + C2H5OH → CH3COOCH3 + H2O (1)
0,24 0,24 0,24 (mol)
Đề bài: 0,3 0,32 (mol)
⇒ hiệu suất tính theo axit
H% = 0,24/0,3.100% = 80%
⇒ Đáp án B.
Ví dụ 3 : Khi triển khai phản ứng este hoá 1 mol CH3COOH cùng 1 mol C2H5OH, lượng este lớn nhất thu được là 2/3 mol. Để đạt hiệu suất cực to là 90% (tính theo axit) khi tiến hành este hoá 1 mol CH3COOH đề xuất số mol C2H5OH là (biết những phản ứng este hoá thực hiện ở cùng nhiệt độ)
A. 0,342. B. 2,925. C. 2,412. D. 0,456.
Hướng dẫn giải:
Phương trình bội phản ứng :
CH3COOH + C2H5OH → CH3COOC2H5 + H2O (1)
bđ: 1 1 (mol)
pư: 2/3 2/3 2/3 2/3 (mol)
cb: 1/3 1/3 2/3 2/3 (mol)
Tại thời gian cân bằng, thể tích dung dịch là V
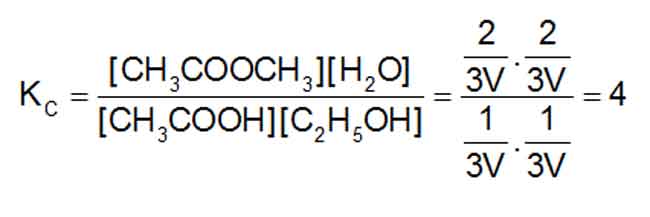
Gọi x là số mol C2H5OH buộc phải dùng, công suất phản ứng tính theo axit buộc phải số mol axit phản bội ứng là 0,9 mol.
Phương trình bội nghịch ứng :
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
bđ: 1x (mol)
pư:0,9 0,9 0,9 0,9 (mol)
cb: 0,1 x – 0,9 0,9 0,9 (mol)
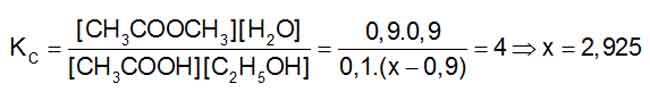
⇒ Đáp án B.
Dạng 6: Điều chế ancol etylic
Phương pháp:
(C6H10O5)n + n
H2O lên men rượu→ n
C6H12O6
C6H12O6 lên men rượu→ 2C2H5OH + 2CO2
Độ rượu (độ ancol) là số ml rượu (ancol) nguyên chất tất cả trong 100 ml dung dịch hỗn hợp rượu và nước.
Ví dụ minh họa
Ví dụ 1 : Lên men m gam glucozơ với công suất 90%, lượng khí CO2 hình thành hấp thụ không còn vào dung dịch nước vôi trong, chiếm được 10 gam kết tủa. Cân nặng dung dịch sau bội phản ứng bớt 3,4 gam so với cân nặng dung dịch nước vôi vào ban đầu. Quý hiếm của m là :
A. 20,0. B. 30,0. C. 13,5. D. 15,0.
Hướng dẫn giải:
Phương trình phản ứng :
C6H12O6 lên men rượu→ 2C2H5OH + 2CO2 (1)
CO2 + Ca(OH)2 → Ca
CO3 + H2O (2)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (3)
mdung dịch sút = m
Ca
CO3 kết tủa – m
CO2
⇒ m
CO2 = m
Ca
CO3 – mdung dịch sút = 6,6g ⇒ n
CO2 = 0,15 mol
Theo (1) ta tất cả :
n
C6H12O6 pư = 50% n
CO2 = 0,075 mol
Vì công suất phản ứng lên men là 90% đề nghị lượng glucozơ bắt buộc cho làm phản ứng là :
n
C6H12O6 pư = 0,075 : 90% = 1/12 mol ⇒ m = 1/12.180 = 15g
⇒ Đáp án D.
Ví dụ 2 : Đi từ 150 gam tinh bột sẽ điều chế được từng nào ml ancol etylic 46o bằng cách thức lên men ancol? cho thấy thêm hiệu suất bội phản ứng đạt 81% cùng d = 0,8 g/ml.
A. 46,875 ml. B. 93,75 ml. C. 21,5625 ml. D. 187,5 ml
Hướng dẫn giải:
Khối lượng tinh bột tham gia phản ứng là: 150.81%=121,5 gam.
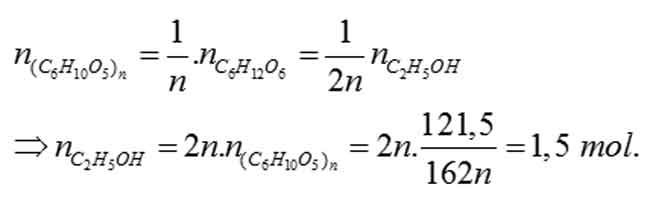
Thể tích ancol nguyên hóa học là :
Vrượu nguyên chất = 1,5.46/0,8 = 86,25ml ⇒ Vrượu = 86,25/46 .100= 187,5ml
⇒ Đáp án D.



Phương pháp giải bài xích tập làm phản ứng đốt cháy ancol


BÀI TOÁN ĐỐT CHÁY ANCOL
Phương pháp giải nhanh
+ Số mol H2O > số mol CO2 suy ra ancol là ancol no
+ Số mol ancol no = Số mol H2O – số mol CO2
+ vận dụng định nguyên lý bảo toàn thành phần oxi có
a. Số mol ancol + 2. Số mol O2 = Số mol H2O +2. Số mol CO2Chú ý:
– phản nghịch ứng đốt cháy của ancol có điểm lưu ý tương tự bội phản ứng đốt cháy hiđrocacbon tương ứng:
+ giả dụ đốt cháy ancol mang lại n
H2O> n
CO2thì ancol mang đốt cháy là ancol no cùng n
Ancol= n
H2O– n
CO2:
Cn
H2n+2Ox→ n
CO2+ (n + 1)H2O
+ ví như đốt cháy ancol đến n
H2O> 1,5.n
CO2thì ancol là CH3OH. Chỉ gồm CH4và CH3OH có tính chất này (không nói amin):
CH3OH→ CO2+ 2H2O
+ ví như đốt cháy ancol mang đến n
CO2= n
H2Othì ancol đó tất cả dạng Cn
H2n
Ox:
Cn
H2n
Ox→ n
CO2+ n
H2OCâu 1 : Đốt cháy hoàn toàn một ancol đa chức, mạch hở Xthu được H2O với CO2 với tỉ lệ thành phần số mol tương ứng là 3:2. Cách làm phân tử của X là
A. C2H6O2 B. C2H6O C. C4H10O2 D. C3H8O2
Lời giải
H2O : CO2 = 3:2 đề nghị Số mol H2O > số mol CO2 suy ra ancol X no
Gọi CTPT của X là Cn
H2n+2Ox. Ta bao gồm n = = 2 buộc phải CTPT của X là C2H6Ox
Vì ancol X là ancol nhiều chức buộc phải x = 2 là tán đồng . Chọn đáp án ACâu 2 : Đốt cháy trọn vẹn hỗn thích hợp M bao gồm 2 ancol X, Y là đồng đẳng tiếp đến nhau, thu được 0,3 mol CO2 cùng 0,425 mol H2O. Mặt khác, đến 0,25 mol các thành phần hỗn hợp M tính năng với na dư, thu được không tới 0,15 mol H2. Công thức phân tử của X, Y là
A. C3H6O, C4H8O B. C2H6O, C3H8O
C. C2H6O2, C3H8O2 D. C2H6O, CH4O
Lời giải
Vì số mol H2O > số mol CO2 bắt buộc X, Y là 2 ancol no
nancol = 0,425 – 0,3 = 0,125 mol.Số nhóm OH trong ancol
Ancol là 1-1 chức. Số nguyên tử = = 2,4 Ancol X, Y là C2H6O, C3H8O
Chọn giải đáp B
Câu 3 : X là một trong những ancol no, mạch hở. Đốt cháy hoàn toàn 0,05 mol X đề nghị 5,6 gam oxi, thu được khá nước với 6,6 gam CO2. Phương pháp của X là
A. C2H4(OH)2 B. C3H7OH C. C3H5(OH)3 D. C3H6(OH)2
Lời giải
Vì X là ancol no đề nghị số mol H2O = nancol +số mol CO2 = 0,05 + = 0,2 mol
Số nguyên tử C = = 3 cùng số team OH vào X là a thì áp dụng định phương tiện bảo toàn nguyên tố bao gồm : a.số mol ancol + 2. Số mol O2 = Số mol H2O +2. Số mol CO2
a . 0,05 + 2 . 0,175 = 0,2 + 2.0,15 a = 3 đề nghị CTPT của X là C3H5(OH)3
Chọn giải đáp C
Câu 4 : Đốt cháy hoàn toàn một ancol X thu được CO2 và H2O gồm tỉ lệ số mol tương xứng là 3:4. Thể tích khí oxi cần dùng để đốt cháy X bởi 1,5 lần thể tích khí CO2 chiếm được (ở cùng điều kiện). Cách làm phân tử của X là
A. C3H8O2 B. C3H8O3 C. C3H4O D. C3H8O
Lời giải
H2O : CO2 = 4:3 yêu cầu Số mol H2O > số mol CO2 suy ra ancol X no
Gọi CTPT của X là Cn
H2n+2Ox. Ta bao gồm n = = 3 cần CTPT của X là C3H8Ox
Phương trình cháy C3H8Ox + (5 – )O2 3CO2 + 4H2O
1,5 1
Nên 5 – = 1,5.3 x = 1 vậy X là C3H8O. Chọn câu trả lời D
Câu 5 : Đốt cháy hoàn toàn 0,2 mol một ancol X no, mạch hở nên vừa đủ 17,92 lít khí oxi (đktc). Mặt khác nếu cho 0,1 mol X tác dụng vừa đủ với m gam Cu(OH)2 thì tạo ra thành hỗn hợp có màu xanh lá cây lam. Quý giá của m và tên thường gọi của X khớp ứng là
A. 4,9 gam và propan – 1,2 – điol B. 9,8 gam cùng propan – 1,2 – điol
C. 4,9 gam cùng glixerin D. 4,9 gam cùng propan – 1,3 – điol
Lời giải
Ancol X no, mạch hở gồm CTPT là Cn
H2n+2Oa
Cn
H2n+2Oa + O2 n
CO2 + (n+1)H2O
= . 0,2 3n = 7 + a .
Mặt không giống X là ancol nhiều chức vì chưng làm tan Cu(OH)2
Nên chỉ có giá trị a = 2 , n = 3 là thoả mãn
Vậy X là C3H6(OH)2 cùng với CTCT là CH3 – CHOH – CH2OH : propan – 1,2 – điol
Phương trình phản bội ứng
2C3H6(OH)2 + Cu(OH)2 (C3H7O2)2Cu + 2H2O
0,1 mol 0,05 mol
Vậy m = 0,05 . 98 = 4,9 gam. Chọn đáp án A
Câu 6 : Đốt cháy một lượng ancol no đối chọi chức A được 15,4 gam CO2 với 9,45 gam H2O . Tìm phương pháp phân tử của A ?
Lời giải
Số C của ancol no = = = 2
Vậy A có công thức phân tử là C2H6O
Câu 7:Đốt cháy trọn vẹn một lượng hiđrocacbon A thu được 26,4 gam CO2 và 16,2 gam H2O . Tìm phương pháp phân tử của A ?
Lời giải
( với n
HO = 0,7 mol > n CO= 0,6 mol ) => A là ankan
Số C của ankan = = = 6
Vậy A có công thức phân tử là C6H14
BÀI TOÁN ĐIỀU CHẾ ANCOL ETYLIC
Phương pháp giải nhanh
+ Ta tất cả sơ đồ (C6H10O5)n n
C6H12O6 2n
C2H5OH + 2n
CO2
Tinh bột hoặc xenlulozơ glucozơ
Câu 1 : Lên men dung dịch đựng 300 gam glucozơ nhận được 92 gam ancol etylic. Hiệu suất quá trình lên men tạo nên thành ancol etylic là
A. 40% B. 60% C. 80% D. 54%
Lời giải
Ta bao gồm sơ vật C6H12O6————> 2C2H5OH
1 mol 2 mol
Khối lượng glucozơ phản ứng là : 1 . 180 = 180 gam. Vậy H = = 60%
Chọn giải đáp B
Câu 2 : Lên men trọn vẹn m gam glucozơ thành ancol etylic. Toàn bộ khí CO2 xuất hiện trong quá trình này được kêt nạp hết vào dung dịch Ca(OH)2 dư tạo nên 40 gam kết tủa. Ví như hiệu suất quá trình lên men tạo thành thành ancol etylic là 75% thì quý hiếm của m là
A. 60 B. 48 C. 30 D. 58
Lời giải
Ta gồm sơ vật dụng C6H12O6 2C2H5OH + 2CO2
0,2 mol 0,4 mol
CO2 + Ca(OH)2 Ca
CO3 + H2O
0,4 mol = 0,4 mol
Khối lượng glucozơ phản bội ứng là : 0,2 . 180 = 36 g.
Vì H = 75% buộc phải m = = 48 g
Chọn câu trả lời B
Câu 3 : Lên men m gam tinh bột thành ancol etylic. Tổng thể khí CO2 có mặt trong quá trình này được hấp thụ trọn vẹn vào dung dịch Ca(OH)2, tạo nên 550 gam kết tủa cùng dung dịch X. Đun kĩ hỗn hợp X thu thêm được 100 g kết tủa. Giả dụ hiệu suất quy trình lên men tạo ra thành ancol etylic là 81% thì cực hiếm của m là
A. 550 B. 810 C. 650 D. 750
Lời giải
Ta bao gồm sơ đồ vật (C6H10O5)n 2n
C2H5OH + 2n
CO2
3,75/n mol 7,5 mol
CO2 + Ca(OH)2 Ca
CO3 + H2O
5,5 mol = 5,5 mol
2CO2 + Ca(OH)2 Ca(HCO3)2 Ca(HCO3)2 Ca
CO3 + H2O + CO2
2 mol 1 mol 1 mol = 1 mol
Khối lượng tinh bột phản nghịch ứng là : 162n . = 607,5 gam
Vì H = 81% đề xuất m = = 750 gam. Chọn câu trả lời D
Câu 4 : Lên men m gam tinh bột thành ancol etylic. Toàn thể khí CO2 xuất hiện trong quy trình này được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, tạo ra 330 gam kết tủa cùng dung dịch X. Trọng lượng dung dịch X giảm sút so với khối lượng nước vôi trong thuở đầu là 132 g. Giả dụ hiệu suất quy trình lên men chế tạo thành ancol etylic là 90% thì quý giá của m là
A. 486 B. 297 C. 405 D. 324
Lời giải
Ta tất cả sơ đồ vật (C6H10O5)n 2n
C2H5OH + 2n
CO2
2,25/n mol 4,5 mol
Khối lượng dung dịch giảm = mkết tủa – m
CO m
CO= 330 – 132 = 198 gam
Khối lượng tinh bột phản nghịch ứng là : 162n . = 364,5 gam
Vì H = 90% phải m = = 405 gam. Chọn câu trả lời C
Câu 5: mang đến m gam tinh bột lên men thành ancol etylic với hiệu suất 81%. Toàn bộ lượng CO2 hiện ra được hấp thụ hoàn toàn vào hỗn hợp Ca(OH)2, thu được 550 gam kết tủa và dung dịch X. Đun kĩ dung dịch X thu thêm được 100 gam kết tủa. Quý giá của m là
A. 550 B. 650 C. 750 D. 810Lời giải
Lượng CO2 có mặt được hấp thụ trọn vẹn vào dung dịch Ca(OH)2, thu được kết tủa với dung dịch X, đun X lại chiếm được kết tủa
=> tất cả muối HCO3– được tạo nên thành, ta có những pt
C6H10O5 ——> C6H12O6 ——–> 2C2H5OH + 2CO23,75 CO2 + Ca(OH)2 ——-> Ca
CO3 + H2O5,5 2CO2 + Ca(OH)2 ———> Ca(HCO3)22 Ca(HCO3)2 —————> Ca
CO3 + CO2 + H2O1 => n
CO2 = 5,5 + 2 = 7,5 molm = (3,75.162) : 0,81 = 750 gam=> Đáp án CCâu 6: Ancol etylic được pha trộn từ tinh bột bằng cách thức lên men cùng với hiệu suất cục bộ quá trình là 90%. Hấp thụ tổng thể lượng CO2 ra đời khi lên men m gam tinh bột vào nước vôi trong, thu được 247,5 gam kết tủa với dung dịch X. Biết cân nặng X sụt giảm so với cân nặng nước vôi trong lúc đầu là 99 gam. Giá trị của m là
A. 200,475 B. 222,75C. 303,75 D. 273,375Lời giải
(C6H10O5)n + n
H2O → n
C6H12O6
C6H12O6 → 2C2H5OH + 2CO2
mdd ↓ = m Ca
CO3 – m
CO2 đang hấp thụ
=> m CO2 = 247,5 – 99 = 148,5 gam tương tự 3,375 mol khí CO2
n C6H12O6 = n CO2 : 2 = 1,6875 mol
n(C6H10O5)n lt = 1,6875/n mol
m(C6H10O5)n lt = 1,6875/n x 162n = 273,375 gam
m(C6H10O5)n tt = 273,375 : 90% = 303,75 gam
=> Đáp án C
BÀI TẬP ANCOL BỊ OXI HÓA
1. Ancol bị oxi hóa bươi Cu
O, đun nóng
Phương pháp giải nhanh
+ áp dụng định hình thức bảo toàn trọng lượng và yếu tắc ta có
nancol = nanđehit = n
Cu
O = n
Cu = =
+ thành phầm gồm anđehit, nước, ancol dư cho công dụng với mãng cầu dư thì
nancol bđ = 2n
H
+ thành phầm cho chức năng với hỗn hợp Ag
NO3 / NH3 dư thì
– nếu như n
Ag ancol thì trong 2 ancol có 1 ancol bậc 1 cùng 1 ancol bậc cao
– nếu như n
Ag = 2nancol thì trong 2 ancol cả hai ancol phần đông là ancol bậc 1 khác CH3OH
– nếu như n
Ag > 2nancol thì trong 2 ancol có 1 ancol là ancol bậc 1 (RCH2OH) khác CH3OH cùng 1 ancol là CH3OH
Ta có sơ vật R – CH2OH R – đến 2Ag
x mol 2x mol
CH3OH HCHO 4Ag
y mol 4y mol
Sau đó lập hệ phương trình giải x, y rồi tính cân nặng 2 ancol tìm kiếm được CTPT của ancol
Câu 1 : Oxi hoá ancol đối kháng chức X bởi Cu
O (đun nóng), có mặt một sản phẩm hữu cơ Y độc nhất vô nhị là xeton (tỉ khối của Y đối với hiđro bằng 29). Công thức cấu trúc của X là
A. CH3 – CHOH – CH3 B. CH3 – CH2 – CH2OH
C. CH3 – CH2 – CHOH – CH3 D. CH3 – teo – CH3
Lời giải
Vì oxi hoá ancol đơn chức X tạo thành xeton Y nên X là ancol đối chọi chức bậc 2
Ta có sơ đồ R – CHOH – R’ + Cu
O R – co – R’ + Cu + H2O
MY = R + 28 + R’ = 29. 2 = 58 R + R’ = 30 .Chỉ tất cả R = 15, R’ = 15 là thoả mãn
Nên xeton Y là CH3 – teo – CH3 . Vậy CTCT của ancol X là CH3 – CHOH – CH3
Chọn lời giải A
Câu 2 : đến m gam một ancol no, đối chọi chức X qua bình Cu
O dư đun nóng. Sau khi phản ứng hoàn toàn, khối lượng chất rắn trong bình giảm 0,32 gam. Hỗn hợp hơi thu được có tỉ khối với hiđro là 15,5. Cực hiếm của m là
A. 0,92 g B. 0,32 g C. 0,64 g D. 0,46 g
Lời giải
Áp dụng định lao lý bảo toàn khối lượng và yếu tắc ta có
nancol = nanđehit = = = 0,02 mol
Ta có sơ vật R – CH2OH + Cu
O R – mang đến + Cu + H2O
0,02 mol 0,02 mol 0,02 mol
Ta bao gồm = = 15,5 . 2 = 31
Suy ra R = 15 đề nghị ancol X là CH3OH
Vậy trọng lượng ancol X là : m = 0,02 . 32 = 0,64 gam. Chọn lời giải C
Câu 3 : đến m gam các thành phần hỗn hợp X gồm 2 ancol no, đơn chức, sau đó nhau trong dãy đồng đẳng tác dụng với Cu
O dư đun nóng, chiếm được một hỗn hợp rắn Z với một hỗn hợp hơi Y (có tỉ khối so với hiđro là 13,75). Cho toàn bộ Y phản ứng với cùng 1 lượng dư Ag2O (hoặc Ag
NO3) trong hỗn hợp NH3 đun nóng, sinh ra 64,8 gam Ag. Cực hiếm của m là
A. 7,8 g B. 8,8 g C. 7,4 g D. 9,2 g
Lời giải
Ta có sơ vật dụng – CH2OH + Cu
O – mang đến + Cu + H2O
Hỗn vừa lòng hơi Y gồm các anđehit và H2O với số mol đều bằng nhau nên
Y = = 13,75 . 2 = 8. Nhưng mà 2 ancol là đồng đẳng thường xuyên nên 2 ancol là CH3OH với C2H5OH. Bởi = 8 = bắt buộc 2 ancol bao gồm số mol đều nhau và bởi x mol
Ta gồm sơ đồ vật CH3 – CH2OH CH3 – mang đến 2Ag
x mol 2x mol
CH3OH HCHO 4Ag
x mol 4x mol
n
Ag = 6x = = 0,6 x = 0,1 mol. Vậy m = 0,1 . 46 + 0,1 . 32 = 7,8 gam
Chọn lời giải A
Câu 4 : Oxi hoá 0,1 mol ancol etylic chiếm được m gam hỗn hợp Y có axetanddehit, nước với ancol etylic dư. Cho Na dư vào m gam tất cả hổn hợp Y hiện ra V lít hiđro (đktc). Tuyên bố đúng là
A. V = 2,24 lít
B. V = 1,12 lít
C. Năng suất phản ứng oxi hoá ancol là 100%
D. Số mol Na bội nghịch ứng là 0,2 mol
Lời giải
Ta bao gồm nancol bđ = 2n
Hn
H= = 0,05 mol
Vậy V = 0,05 . 22,4 = 1,12 lít . Chọn đáp án B
Câu 5 : Oxi hoá không còn 0,2 mol ancol A, B liên tiếp nhau trong dãy đồng đẳng bởi Cu
O đun nóng được hỗn hợp X tất cả 2 anđehit. Cho X tác dụng với lượng dư dung dịch Ag
NO3/NH3 được 54 gam Ag. Vậy A, B là
A. CH3OH cùng C2H5OH B. C2H5OH và C3H7OH
C. C2H4(OH)2 cùng C3H7OH D. C2H5OH cùng C3H5(OH)3
Lời giải
Vì n
Ag = 0,5 mol > 2nancol buộc phải 2 ancol A, B là CH3OH với C2H5OH
Chọn đáp án A
Câu 6 : hỗn hợp X có ancol metylic với một ancol no, đơn chức A mạch hở. Mang đến 2,76 gam X chức năng hết với na dư thu được 0,672 lít hiđro (đktc), ngoài ra oxi hoá hoàn toàn 2,76 gam X bởi Cu
O dư nung lạnh thu được hỗn hợp anđehit. Cho toàn bộ lượng anđehit này tính năng với lượng dư dung dịch Ag
NO3/NH3 dư nhận được 19,44 gam Ag. Công thức cấu trúc của A là
A. C2H5OH B. CH3CH2CH2OH
C. (CH3)2CHOH D. CH3CH2CH2CH2OH
Lời giải
Ta gồm nancol X = 2n
H= 2 . 0,03 = 0,06 mol
Ta bao gồm sơ đồ R – CH2OH R – mang đến 2Ag
x mol 2x mol
CH3OH HCHO 4Ag
y mol 4y mol
Có n
Ag = 2x + 4y = 0,18 (1)và nancol X = x + y = 0,06 (2)
Từ (1) và (2) suy ra x = y = 0,03 mol. Phương diện khácmancol X = 0,03 . 32 + 0,03 . (R + 31) = 2,76 R = 29. Vậy ancol A là CH3CH2CH2OH. Chọn lời giải B
Câu 7 : Oxi hoá 1,2 gam CH3OH bằng Cu
O nung nóng, sau một thời gian thu được lếu hợp thành phầm X (gồm HCHO, H2O và CH3OH dư). Cho toàn cục X chức năng với lượng dư hỗn hợp Ag
NO3/NH3 được 12,96 gam Ag. Năng suất của phản ứng oxi hoá CH3OH là
A. 76,6% B. 80,0% C. 65,5% D. 70,4%
Lời giải
Ta tất cả sơ đồ dùng CH3OH HCHO 4Ag
0,03 mol 0,03mol 0,12 mol
Khối lượng CH3OH phản nghịch ứng là : 0,03 . 32 = 0,96 gam
Hiệu suất bội phản ứng oxi hoá là : = 80,0%. Chọn giải đáp B
Câu 8 : Oxi hoá không hoàn toàn ancol isopropylic bằng Cu
O nung nóng, thu được chất hữu cơ X. Tên gọi của X là
A. Propanal B. Metyl vinyl xeton
C. Metyl phenyl xeton D. đimetyl xeton
Lời giải
Chọn lời giải D
ANCOL TÁC DỤNG VỚI Na
Phương pháp giải nhanh
+ giả dụ đề cho trọng lượng ancol, cân nặng Na và trọng lượng chất rắn sau bội nghịch ứng thì áp dụng định khí cụ bảo toàn trọng lượng ta có : n
H=
+ ví như đề cho cân nặng ancol, Na bội nghịch ứng không còn và cân nặng chất rắn sau phản nghịch ứng thì vận dụng định chính sách bảo toàn khối lượng ta gồm :
n
Na= = a. N
H(với a là số đội OH)
+ Số đội OH =
Câu 1 : mang đến 15,6 gam tất cả hổn hợp 2 ancol solo chức tiếp nối nhau trong dãy đồng đẳng tác dụng hết với 9,2 gam mãng cầu thu được 24,5 gam hóa học rắn. 2 ancol kia là
A. CH3OH cùng C2H5OH B. C3H7OH và C4H9OH
C. C3H5OH và C4H7OH D. C2H5OH với C3H7OH
Lời giải
áp dụng định hiện tượng bảo toàn khối lượng ta có
n
H= = = 0,15 mol
Gọi bí quyết chung của 2 ancol là OH
OH + na ONa + H2
0,3 mol 0,15 mol
Suy ra = = 52 = 52 – 17 = 35
Mà 2 ancol là đồng đẳng tiếp tục nên 2 ancol bắt buộc là C2H5OH với C3H7OH
Chọn lời giải D
Câu 2 : mang đến 18,4 g X bao gồm glixerol và một ancol no đơn chức Y tác dụng với mãng cầu dư thu được 5,6 lít khí hiđro (đktc). Lượng hiđro vày Y sinh ra bởi 2/3 lượng hiđro do glixerol sinh ra. Công thức phân tử của Y là
A. CH3OH B. C2H5OH C. C3H7OH D. C4H9OH
Lời giảiSơ đồ dùng phản ứng
C3H5(OH)3 H2 ROH H2
a mol 1,5a mol b mol 0,5b mol
Ta tất cả phương trình : n
H= 1,5a + 0,5b = = 0,25 (1) với 0,5b = .1,5a (2)
Từ (1) với (2) suy ra a = 0,1 ; b = 0,2 mol
m
X = 0,1 . 92 + 0,2 . (R + 17) = 18,4 R = 29 (C2H5). Vậy ancol Y là C2H5OH
Chọn câu trả lời B
Câu 3 : cho những chất sau :
1. HOCH2CH2OH 2. HOCH2CH2CH2OH 5. CH3CH(OH)CH2OH
3. HOCH2CH(OH)CH2OH 4. CH3CH2OCH2CH3
Những chất tính năng được với Cu(OH)2 là
A. 1, 2, 3, 5 B. 1, 2, 4, 5 C. 1, 3, 5 D. 3, 4, 5
Lời giải
Những chất công dụng được cùng với Cu(OH)2 là rất nhiều chất tất cả 2 đội OH kề nhau
Vậy cần ta chọn đáp án C
Câu 4 : A, B là 2 ancol no solo chức, kế tiếp nhau trong dãy đồng đẳng. Mang lại hỗn hợp gồm 1,6 gam A và 2,3 gam B chức năng hết với mãng cầu thu được 1,12 lít H2 (đktc). A, B có công thức phân tử lần lượt là
A. CH3OH ; C2H5OH B. C2H5OH ; C3H7OH
C. C3H7OH ; C4H9OH D. C4H9OH ; C5H11OH
Lời giải
Gọi bí quyết chung của 2 ancol là OH
OH + na ONa + H2
0,1 mol 0,05 mol
Suy ra = = 39 = 39 – 17 = 22
Mà 2 ancol là đồng đẳng liên tục nên 2 ancol nên là CH3OH cùng C2H5OH
Chọn lời giải A
Câu 5 : đến 1,52 gam tất cả hổn hợp 2 ancol đối chọi chức sau đó nhau trong hàng đồng đẳng tính năng với Na trọn vẹn thu được 2,18 gam chất rắn. 2 ancol đó là
A. CH3OH với C2H5OH B. C3H7OH và C4H9OH
C. C3H5OH cùng C4H7OH D. C2H5OH với C3H7OH
Lời giải
áp dụng định luật pháp bảo toàn cân nặng ta có :
n
Na= = = 0,03 mol
Gọi cách làm chung của 2 ancol là OH
OH + mãng cầu ONa + H2
0,03 mol 0,03 mol
Suy ra = = 50,67 = 50,67 – 17 = 36,67
Mà 2 ancol là đồng đẳng liên tiếp nên 2 ancol nên là C2H5OH với C3H7OH
Chọn lời giải D
Câu 6 : cho 9,2 gam các thành phần hỗn hợp ancol propylic với ancol đơn chức B tính năng với na dư sau làm phản ứng nhận được 2,24 lít H2 (đktc). Phương pháp của B là
A. CH3OH B. C2H5OH
C. CH3CH(OH)CH3 D. CH2 = CH – CH2OH
Lời giải
Gọi phương pháp chung của 2 ancol là OH
OH + mãng cầu ONa + H2
0,2 mol 0,1 mol
Suy ra = = 46 = 46 – 17 = 29
Mà có một ancol là C3H7OH đề nghị ancol còn sót lại phải là CH3OH
Chọn câu trả lời A
Câu 7 : đến 10 ml dung dịch ancol etylic 46o tác dụng với na dư. Xác định thể tích H2 tạo ra thành? (biết khối lượng riêng của ancol etylic là 0,8 g/ml)
A. 2,128 lít B. 0,896 lít C. 3,360 lít D. 4,256 lít
Lời giải
Thể tích C2H5OH nguyên chất là : = 4,6 ml
Khối lượng C2H5OH nguyên chất là : 4,6 . 0,8 = 3,68 (g)
Thể tích H2O = 10 – 4,6 = 5,4 ml; trọng lượng H2O là : 5,4 . 1 = 5,4 g
Sơ đồ vật phản ứng
C2H5OH H2 H2O H2
mol 0,15 mol mol 0,04 mol
Vậy thể tích H2 nhận được là : (0,04+ 0,15) . 22,4 = 4,256 (lít)
Chọn câu trả lời D
ANCOL TÁCH NƯỚC
1. Ancol tách bóc nước sản xuất anken
Phương pháp giải nhanh
+ Ancol bóc nước tạo nên 1 anken tốt nhất thì ancol chính là ancol no 1-1 chức, bậc 1
+ vận dụng định pháp luật bảo toàn khối lượng có m= m+ m
+ n= n= n
+ tất cả hổn hợp X tất cả 2 ancol tách nước thu được hỗn hợp Y gồm các olefin thì lượng CO2 thu được lúc đốt cháy X bởi khi đốt cháy Y
Câu 1 : Khi tách nước xuất phát từ một chất X bao gồm công thức phân tử C4H10O chế tạo ra thành 3 anken là đồng phân của nhau (tính cả đồng phân hình học). Công thức cấu trúc thu gọn của X là :
A. CH3CH(OH)CH2CH3 B. (CH3)3COH
C. CH3OCH2CH2CH3 D. CH3CH(CH3)CH2OH
Lời giải
Loại dần câu trả lời không phù hợp; loại B cùng C vì chưng B, C không bị tách nước
Loại D vày D chỉ bao gồm một hướng bóc nên ko thể tạo nên 3 anken
Vậy chọn lời giải A
Câu 2 : Khi tiến hành phản ứng tách nước so với ancol X, chỉ thu được 1 anken duy nhất. Oxi hoá hoàn toàn một lượng chất X chiếm được 5,6 lít CO2 (đktc) và 5,4 gam H2O. Tất cả bao nhiêu bí quyết cấu tạo phù hợp với X?
A. 5 B. 4 C. 2 D. 3
Lời giải
X bị tách bóc nước chế tạo ra 1 anken X là ancol no, đơn chức với chỉ có một hướng tách
Công thức phân tử của X là Cn
H2n+1OH ;
Có nancol = n
HO – n
CO= – = 0,05 mol
Và n = = 5 . Bắt buộc công thức phân tử của X là C5H11OH
Công thức cấu trúc của X là
CH3 – CH2 – CH2 – CH2 – CH2OH ; CH3 – CH(CH3) – CH2 – CH2OH
CH3 – CH2 – CH(CH3) – CH2OH ; Chọn lời giải D
Câu 3 : tách nước hoàn toàn từ hỗn hợp X có 2 ancol A, B ta được hỗn hợp Y gồm những olefin. Nếu đốt cháy hoàn toàn hỗn thích hợp X thì nhận được 1,76 g CO2. Khi đốt cháy trọn vẹn Y thì tổng khối lượng nước và CO2 tạo ra là
A. 2,94 g B. 2,48 g C. 1,76 g D. 2,76 g
Lời giải
Áp dụng định phép tắc bảo toàn nhân tố cacbon ta có
Lượng CO2 thu được lúc đốt cháy Y bằng khi đốt cháy X = = 0,04 mol
Mà Y là lếu hợp những olefin buộc phải số mol H2O = số mol CO2 = 0,04 mol
Vậy tổng trọng lượng CO2 cùng H2O chiếm được là : 0,04 . 18 + 1,76 = 2,48 g
Chọn lời giải B
Câu 4 : cho những ancol sau :
(1) CH3CH2OH (2) CH3CHOHCH3
(3) CH3CH2CH(OH)CH2CH3 (4) CH3CH(OH)C(CH3)3
Dãy gồm những ancol khi tách nước từ từng ancol chỉ cho một olefin nhất là
A. 1, 2 B. 1, 2, 3 C. 1, 2, 4 D. 1, 2, 3, 4
Lời giải
Chọn đáp án CCâu 5 : cho dãy gửi hoá sau : CH3CH2CH2OH X Y
Biết X, Y là sản phẩm chính. Vậy công thức cấu trúc của X với Y theo lần lượt là
A. CH3 – CH = CH2, CH3CH2CH2OH B. CH3 – CH = CH2, CH3CH2CH2OSO3H
C. CH3 – CH = CH2, CH3CHOHCH3 D. C3H7OC3H7, CH3CH2CH2OSO3H
Lời giải
Chọn giải đáp C
Câu 6 : đến sơ đồ gửi hoá sau :
Butan – 2 – ol X Y Z
Trong kia X, Y, Z là sản phẩm chính. Cách làm của Z là
A. CH3 – CH(Mg
Br) – CH2 – CH3 B. (CH3)3C – Mg
Br
C. CH3 – CH2 – CH2 – CH2 – Mg
Br D. (CH3)2CH – CH2 – Mg
Br
(Trích đề thi TSCĐ – B – 2009)
Lời giải
Chọn giải đáp A2. Ancol bóc nước chế tạo ra ete
Phương pháp giải nhanh
+ hỗn hợp 2 ancol bóc nước tạo ra 3 ete, 3 ancol tách nước tạo ra 6 ete
+ áp dụng định cơ chế bảo toàn cân nặng có mancol = mete + mnước
+ nete = nnước = nancol
+ các ete có số mol đều b









